2018 yılının Nobel Kimya ödülleri biyokimya alanında geliştirdikleri ve oldukça yoğun olarak kullanılan biyomoleküler mühendislik yaklaşımları nedeniyle üç farklı bilim insanı arasında bölüştürüldü. İlk başta tamamen birbirinden farklı yöntemler gibi gözükse de aslında geliştirilen iki tekniğin de ortaklaşa kullandığı bir yaklaşım var: Laboratuvarda moleküler evrim.
Ödülün ilk yarısı, Kaliforniya Teknoloji Enstitüsü’nden Dr. Frances H. Arnold’a geliştirdiği “Enzimlerin Yönlendirilmiş Evrimi” adlı yaklaşımından dolayı verildi. Ödülün kalan yarısı ise Dr. George P. Smith ve Dr. Gregory P. Winter arasında, hedeflenen bir moleküle afinite gösterebilen peptitlerin (kısa aminoasit dizisi) ve proteinlerin seçilmesi ya da yeni antikorların geliştirilmesi amacıyla, biyomoleküler kütüphanelerin oluşturulmasını sağlamak üzere geliştirdikleri “faj –bakterileri enfekte eden virüsler- gösterimi” adı verilen teknikten dolayı paylaştırıldı.
Laboratuvarda moleküler evrim yaklaşımının izlediği temel basamaklar kısaca şöyle sıralanabilir:
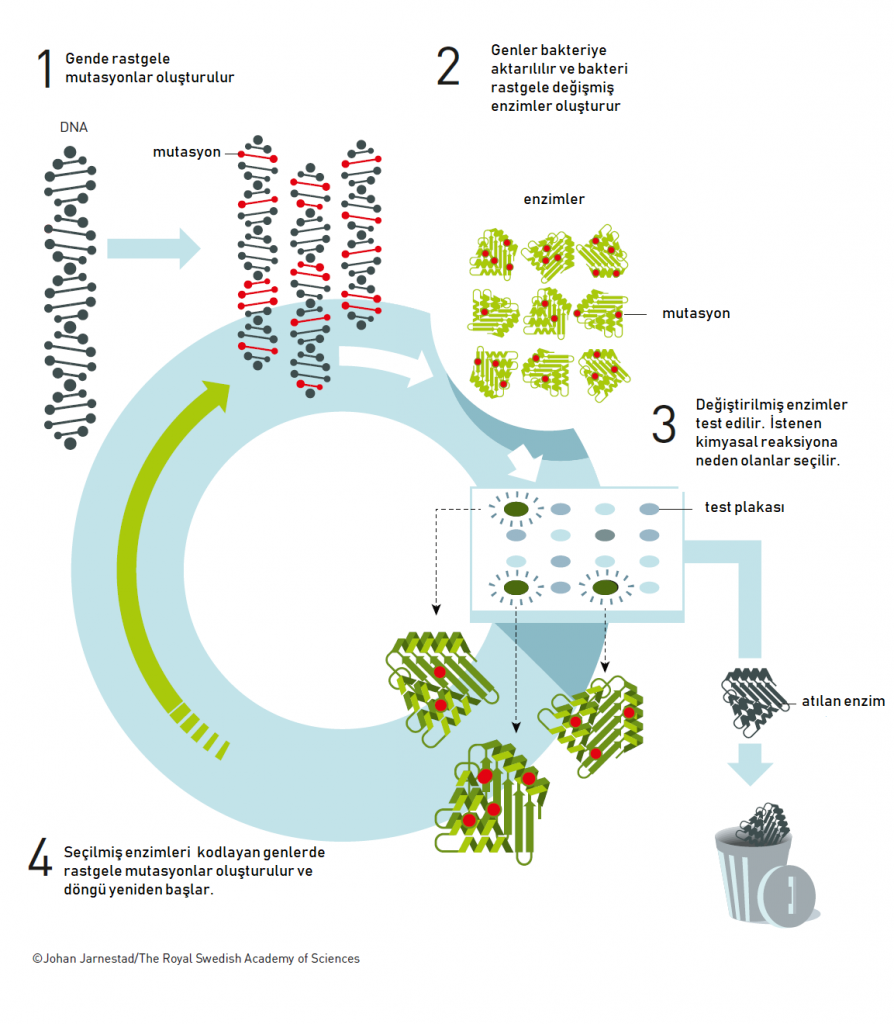
- Rastgele mutasyonların oluşumu ile moleküler çeşitliliğin sağlanması ve bir moleküler kütüphane oluşturulması.
- Oluşturulan mutant kütüphanelerden, tanımlanan bir işlevselliğe sahip moleküllerin seçilmesi amacıyla seçici bir baskı uygulanması. Seçici baskı, istenen işlevi sağlayan moleküllerin öne çıkmasını sağlar. Uygulanan seçici baskının, her bir takip eden seçilim basamağında daha da artırılarak önceki basamakta seçilmiş moleküller arasından en işlevsel olanın seçilimine yönelik tekrar edilmesi.
- Elde edilen seçilmiş moleküllerden işlevsellikleri beklenilene en yakın olanların karakterize edilmeleri.
Proteinler başta olmak üzere pek çok biyomolekülün, doğanın araç kutusunda yer alan en önemli bileşenler olduğunu söylemek yanlış olmaz. Ancak bu moleküller, endüstriyel ve tıbbi uygulamalar için her zaman bizim ihtiyaçlarımızı karşılamayabilirler. Bunun nedeni doğanın, bizim endüstriyel, tıbbi ihtiyaçlarımızı umursamaması ve kendi araçlarını kendi seçilim mekanizmaları ile kendi ihtiyaçlarına yönelik geliştirmiş olmasıdır. Ancak iyi haber şu ki, bu süreçlerde muazzam bir bilgi birikimi var. Bilim insanları, bilimsel yöntemler aracılığı ile bu kuralları ve bilgiyi öğrenerek kendi araç kutumuza yeni molekülleri eklemenin yollarını arıyorlar.
Örneğin, çok düşük sıcaklıklarda çalışan, kloroform gibi sıvılarda aktivite gösteren ya da doğada var olan herhangi bir enzimin tepkimeye girmediği moleküllere aktivite gösteren enzimlerimiz olsa, pek çok konuda daha çevreci yaklaşımlar ortaya konabilirdi. Medikal ve endüstriyel ihtiyaçlarımız için ucuza çözümler üretilebilirdi.
İşte bu noktadan yola çıkan Dr. Arnold da evrimsel süreçleri andırır bir yaklaşımla, aynen doğanın yaptığı gibi, var olan bir enzimi kodlayan DNA parçaları üzerinde rastgele mutasyonlar oluşturmak suretiyle ilgili enzimi farklı mutasyonlar içerecek şekilde kodlayan DNA dizileri oluşturdu. Sonraki aşamada ise oluşturulan bu kütüphaneyi hedeflenen enzime dönüştürebilen organizmalara (ilk basamakta bakterilere) aktararak her farklı bakterinin, hedef enzimin mutantlarını taşımasını sağladı. Son olarak tanımlanan seçici işlevselliğe göre en iyi aktiviteyi gösteren “süper enzimleri” saptadı.
Ödülün diğer yarısına layık görülen bilim insanları ise, enzimlerin yönlendirilmiş evriminden daha farklı olarak, hedef bir moleküle (bir protein, küçük molekül vs.) yüksek bağlanma etkinliğine sahip peptitlerin seçilmesini ya da yeni proteinlerin geliştirilmesini (mesela antikorlar) hedefleyen bir yöntem geliştirdi.
Dr. Arnold’ın yaklaşımından farklı olarak Dr. Smith ve arkadaşları, biyomoleküler kütüphanelerini bir enzim ya da protein üzerinden değil bir virüs üzerinden oluşturdular.
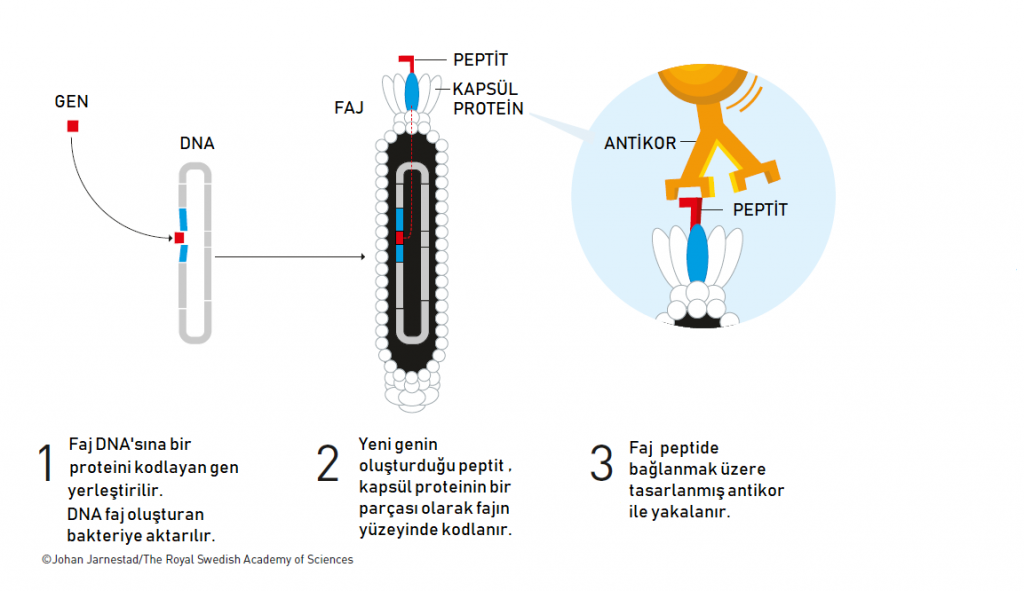
Dr. Smith, faj parçacıkları üzerinde yer alan kılıf proteinlerine bazı yeni peptitler eklemek sureti ile (ve bu peptilerde rastgele mutasyonlar yaratarak) geniş moleküler protein/peptit kütüphaneleri oluşturmanın yolunu açtı. Bu kütüphaneler, hedef bir moleküle (mesela bir hücresel reseptöre, ya da bir toksine, ya da vücut içerisinde sinyal mekanizmalarını olumsuz etkileyen bir proteine) bağlanabilen moleküllerin seçilmesine olanak sağlıyor.
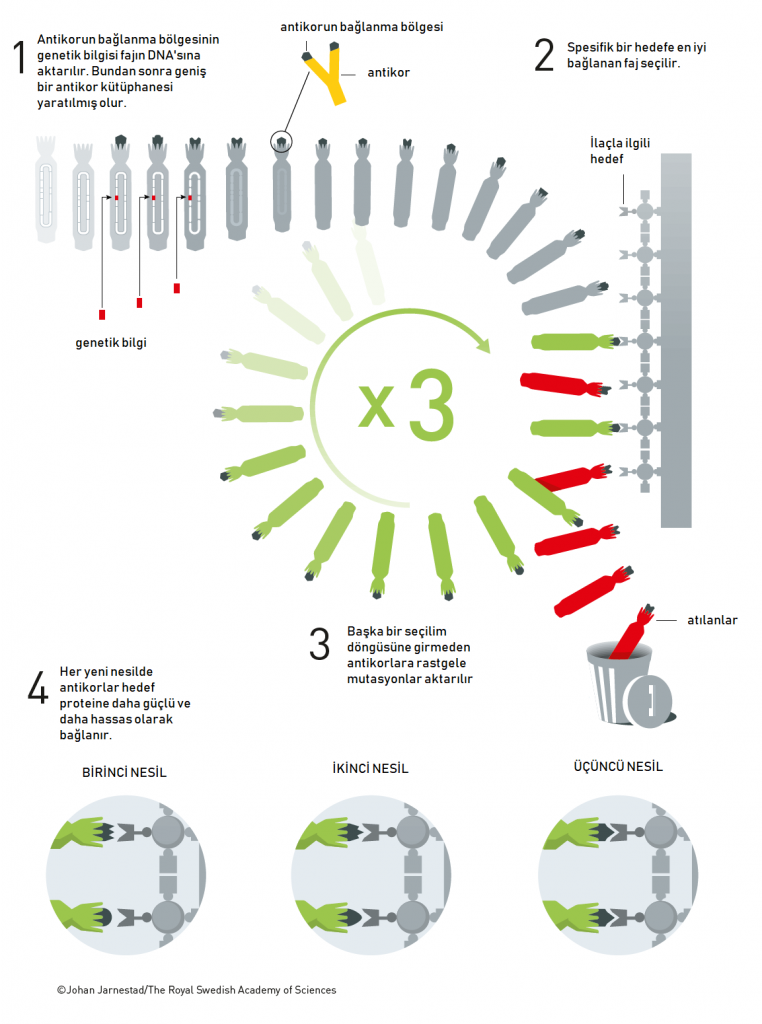
Diyelim ki, hedeflenen reseptör tümör gelişiminde önemli, o zaman elimizdeki peptit molekülü bu reseptöre bağlanarak tümör gelişimini yavaşlatma potansiyeline sahip olabilir. Benzer şekilde diyelim seçtiğimiz peptit nörodejeneratif bir hastalık patolojisinde görülen ve nöral hücrelerin içerisinde birikim oluşturan proteinlere özgül, bu sayede elimizdeki seçili peptiti ilaç adayı olarak kullanarak toksik etkileri olan bu protein birikmesinin önüne geçmek ve hastalığı yavaşlatmak mümkün olabilir.
Son söz olarak, bu senenin Nobel Kimya ödüllerinin, doğadan öğrendiğimiz dersleri, laboratuvar temelli yenilikçi yöntemlere çevirmeyi ve insanlığın faydası için kullanmayı hedefleyen yenilikçi moleküler seçilim teknolojilerine verildiğini söylemek doğru olur. Ortaya konan bu teknolojilerin pek çok biyomedikal uygulamada başarı ile kullanılan yeni moleküllerin ortaya konmasında katkısının üst düzeyde olacağı açıktır.
Urartu Şeker
Bilkent Üniversitesi, Malzeme Bilimi ve Nanoteknoloji Araştırmaları Enstitüsü öğretim üyesi
BAGEP ödülü sahibi
Tüm resimler Nobelprize.org’dan alındı.