Her sene Ekim ayının ilk Pazartesi günü Tıp dünyasının gözleri, Stockholm’deki Karolinska Enstitüsü’nde toplanan Nobel Meclisi’ne (Nobel Assembly) çevrilir. Aylarca büyük bir gizlilikle yürütülen aday gösterme ve değerlendirme sürecinin sonunda alınan karar bu yıl 1 Ekim’de bir basın açıklamasıyla tüm dünyaya duyuruldu. Bu karara göre, 2018 Yılı Nobel Tıp Ödülü “bağışıklığın negatif düzenlemesinin baskılanmasıyla kanser tedavisi konusundaki keşifleri” için James P. Allison ve Tasuku Honjo arasında paylaşıldı.

James P. Allison halen Amerika’daki Texas Üniversitesi, MD Anderson Kanser Merkezi’nde İmmünoloji Bölüm Başkanlığı’nı yürütüyor. Ödüle konu olan çalışmalarına 1990’lı yıllarda Kaliforniya Üniversitesi Berkeley’de yönettiği araştırma grubuyla başlamıştı. Ödülün diğer yarısının sahibi olan Japon bilim insanı Tasuku Honjo ise 1984’ten beri çalışmalarını Kyoto Üniversitesi’nde sürdürüyor.
Peki, bilim dünyasının en önemli ödüllerinden olan Nobel’e layık görülen bu keşifler tam olarak nedir? Bağışıklık sistemimiz ve tümörler arasındaki ilişkiye dair neler biliyoruz? Bağışıklık sistemini kullanarak kanseri tedavi etmek mümkün müdür?
Kanser ve Bağışıklık Sistemi
Kanser, tüm dünyada önemli bir ölüm nedeni. Kötü huylu tümörler, kontrolsüz büyüyerek bulundukları dokuda hasara ve fonksiyon kaybına neden olurlar. Ayrıca uzak organlara da yayılarak benzer etkiler gösterirler. Bağışıklık Sistemi (İmmün Sistem), kanımızda ve dokularımızda gezinerek vücudu yabancı etkenlere karşı koruyan birçok farklı hücre çeşidinden ve bu hücrelerin işlevlerini yerine getirmek veya birbirleriyle haberleşmek için kullandıkları biyolojik moleküllerden oluşan oldukça karmaşık bir ağdır. Bağışıklık sistemi, kendinden olanı yabancı olandan ayırt etme yeteneğine sahiptir. Bu özelliği sayesinde tehditleri algılayıp bunlara karşı etkin bir cevap oluşturarak sağlıklı bir yaşam sürdürmemizi sağlayabilir. Ancak, bağışıklık sistemi tarafından tümörün tanınması, karmaşık ve zorlu bir süreçtir. Buradaki temel nokta; normal hücresel büyümenin ve organizasyonun, kansere dönüşümden ayırt edilebilmesidir. Bu süreç, bağışıklık sisteminin hücreleri tarafından tümörün üzerinde bulunan farklı moleküllerin (antijenlerin) tanınmasını ve bağışıklık yanıtının uyarılmasını içerir. T hücreleri, tümör hücrelerinin doğrudan tanınması ve öldürülmesinde görevli en etkin hücreler arasındadır.
Bağışıklık sisteminin fonksiyonlarından biri de kansere dönüşmeye başlayan hücrelerin büyümesini durdurmak veya zararlı hale gelmeden bunları yok etmektir. Zaten, kansere karşı bağışıklık yanıtlarının en güçlü ve etkili olduğu aşama, kanserleşmenin henüz başladığı erken evrelerdir. Zira tümör büyürken ortaya çıkan genetik veya epigenetik (gen dizisinde oluşan mutasyonlar dışında, DNA’nın kimyasal modifikasyonları sonucunda ortaya çıkan değişiklikler) değişimler, tümörün bağışıklık sistemi tarafından tanınmasını engelleyerek farklı nitelikte kanser hücrelerinin ortaya çıkmasına neden olur. Bağışıklık sistemi tarafından tanınamayan bu hücreler ortadan kaldırılamayarak kontrolsüz bir şekilde çoğalmaya başlarlar. Bu hücreler, bağışıklık sistemi hücrelerinden kaçmayı ve hatta bağışıklık sistemini baskılamayı da başarabilirler. Bu durum, kanser hastalığının ortaya çıkışına ve tedavi edilmezse bireyin ölümüne neden olabilir. İlerlemiş kanserlerin tedavisi çok zordur ve bu alanda yeni tedavi yaklaşımlarına ihtiyaç vardır.
İmmün Kontrol Noktaları
İmmün kontrol noktaları bağışıklık sisteminin kendi kendisini kontrol etmekte kullandığı mekanizmalardır. Bağışıklık sisteminin kendinden olanı yabancıdan ayırt edebildiğinden bahsetmiştik. Virüs, bakteri veya tümör gibi bir tehlikeyi tanıyan bağışıklık sistemi derhal bu tehdidi ortadan kaldırmak üzere aktif hale gelir. T hücreleri organizmanın savunmasında çok kritik rol alan hücrelerdir. T hücreleri, lenf düğümlerinde MHC (Major Histocompatibility Complex) molekülleri üzerinde kendilerine sunulan antijeni, T hücresi reseptörü (TCR – T Cell Receptor) adı verilen protein yapıda bir molekülü kullanarak tanır. Bu şekilde aktivasyon için ilk sinyali alır. İkinci sinyal, T hücresi yüzeyindeki CD28 molekülünün antijeni sunan hücre üzerindeki B7 molekülüne bağlanmasıyla gerçekleşir ve bu iki sinyalin bir araya gelmesiyle T hücresi bu yabancı etkene karşı özgül şekilde aktif hale geçer. Artık onunla savaşmaya hazırdır. Aktive olan ve sayıları artan T hücreleri dolaşıma geçerek hızla tehdidin bulunduğu dokuya gider ve burada saldırıyı başlatır.
Saldırıya hazır hale gelen T hücrelerinde pozitif ve negatif düzenlemeler ortaya çıkar. Pozitif düzenlemeler, T hücrelerini daha saldırgan hale getirir ve etkin bir bağışıklık cevabının ortaya çıkmasını sağlar. Yabancı tehditlere karşı ortaya çıkan bu cevabın aşırı aktivasyonu, sağlıklı hücre ve dokularda yıkıma neden olabileceği için çok iyi kontrol edilmek zorundadır. İşte, bağışıklık sisteminin negatif düzenlenmesi burada devreye girer. Aktif halen gelen T hücrelerinde o ana kadar hücre içinde bulunan CTLA-4 molekülü hücre yüzeyine taşınır. Bu molekül de tıpkı aktivasyon için ikinci uyarıyı sağlayan CD28 molekülü gibi B7 molekülüne bağlanır. Ancak CTLA-4’ün CD28’e bağlanma eğilimi çok daha fazladır ve bu bağlanma sonucunda T hücresi aktivasyonu durdurulabilir. Aktive olmuş T hücreleri işte bu fren sistemi sayesinde görevlerini yerine getirdikten sonra tekrar dinlenme haline dönerler.
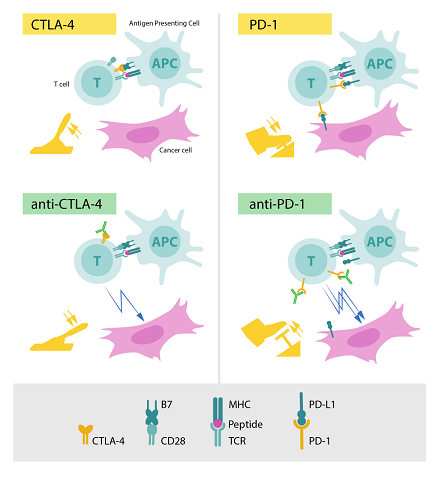
Benzer bir negatif düzenleme sistemi T hücresi üzerinde bulunan PD-1 molekülü için de geçerlidir. PD-1 molekülü de aynı CTLA-4 gibi aktif hale gelen T hücrelerinin yüzeyinde ortaya çıkar ve hedef hücre üzerindeki ligandına bağlandığında T hücre aktivasyonunu durduran bir fren olarak görev yapar. Kanser hücreleri de PD-1’e bağlanacak molekülleri yüzeylerinde bulundurarak bağışıklık sisteminin aktivasyonunu durdurup ve kendilerini yok etmesini önleyebilirler.
İmmünoterapi, tedavi amaçlı olarak bağışıklık sisteminin kullanılmasıdır ve bu amaçla genellikle kanser hücrelerinin hedeflendiği çeşitli yaklaşımlar mevcuttur. James P. Allison ve Tasuku Honjo ‘nun tanımladığı tedavi şeklinin en yenilikçi ve dikkat çekici yönü ise verilen ilaçların hiçbir şekilde kanser hücrelerine yönelik olmayışı. Tedavi tamamıyla bağışıklık sisteminin frenlerinin geçici bir süre durdurulması ve aktivasyonunun devamlılığını hedefliyor. Bu da tedavinin tek bir kanser tipine değil, birçok kansere yönelik kullanılabilmesine olanak sağlıyor
James Allison ve Tasuku Honjo
James P. Allison 1990’lı yıllarda CTLA-4 molekülünün T hücrelerinde bir fren görevi gördüğünü tespit etti ve bu freni ortadan kaldıracak bir başka molekül (antikor) tasarladı. Fareler üzerinde yaptığı ilk deneyler CTLA-4 blokajı yapan antikorlarla tedavi edilen farelerin kanserinin yok olduğunu gösterdi. Devamında insanlar üzerinde çalışmalar başladı ve 2010 yılında bir tür cilt kanseri olan malign melanom hastalarında yapılan kapsamlı bir klinik çalışma umut veren sonuçlar ortaya koydu. Tedavinin ana fikri, ilaç verildiği sürece bağışıklık sisteminin kanser hücrelerine saldırmasının önündeki engelleri kaldırmaktı.
Tasuku Honjo 1992 yılında PD-1 molekülünü buldu ve bu molekülün fonksiyonlarını ilerleyen yıllarda tanımladı. PD-1’in de tıpkı CTLA-4 gibi bir fren işlevi gördüğünü ama farklı mekanizmalarla çalıştığını gösterdi. PD-1’i bloklayan ilaçların kanser tedavisinde olumlu sonuçlar ortaya çıkarttığı önce farelerde, daha sonra ise klinik denemelerde gösterildi. 2012 yılında farklı kanser tiplerinde yapılan klinik çalışmalar, daha önceleri tedavisi mümkün görülmeyen, metastazı olan kanser hastalarında uzun süreli tedavi cevapları sağladı.
James P. Allison ve Tasuku Honjo’nun araştırmaları sayesinde, daha önce çok zor olduğundan bahsettiğimiz ilerlemiş kanseri olan hastaların tedavisi veya yaşam sürelerinin hayal bile edilemeyecek sürelerde uzatılması mümkün hale geldi.
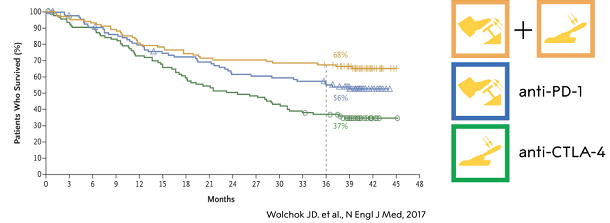
Allison ve Honjo’nun Nobel ödülüne layık görüldüğü 2018 senesi itibariyle anti-CTLA-4 tedavisinin bir hastaya ilk defa verilmesi üzerinden 15 yıl, ilk anti-PD-1 tedavisi üzerinden ise 12 yıl geçmiş bulunuyor. Geçen zaman içerisinde bu tedavileri alan hastaların verdikleri olumlu cevaplar sayesinde kanser tedavisinde büyük ilerleme kaydedildi ve immün kontrol noktalarının bloklanması yeni bir kavram olarak kanser araştırmalarının merkezine oturdu. CTLA-4 ve PD-1’e dayalı tedavilerin tek başlarına çalışmalarının yanı sıra birlikte kullanılmaları durumunda etkilerinin daha da arttığı görülüyor. 2017 yılında yayınlanan son çalışmalara göre malin melanom hastalarında 3 yıllık hayatta kalma oranı anti-CTLA-4 tedavisi alanlarda %37 ve anti-PD-1 tedavisi alanlar %56 iken her iki ilacı birlikte kullanan hastalarda %68 olarak gözlemlenmiş.
Allison ve Honjo’nun bu öncü çalışmalarını takiben halen immün kontrol noktalarının bloklanmasına dayalı birçok yeni tedavi geliştiriliyor. İmmün kontrol noktalarının bloklanması, bu yönüyle doğrudan tümör hücrelerini hedefleyen birçok tedavi yönteminden ayrışıyor; bir destek ve alternatif olarak ön plana çıkıyor. Herhangi bir kanser türüne has bir mekanizmayı değil de genel bir bağışıklık cevabını hedeflediği için test edildiği hemen her kanser türünde olumlu sonuçlar veren bu yeni nesil ilaçlar, radyoterapi, kemoterapi ve cerrahi gibi çok etkili klasik tedavi yöntemlerini destekleyici şekilde kullanılarak kanser hastalarının yaşam umutlarını her geçen gün arttırıyor.
Tolga Sütlü*, Dicle Güç**
*Boğaziçi Üniversitesi Moleküler Biyoloji ve Genetik Bölümü
**Hacettepe Üniversitesi Kanser Enstitüsü