2022 Nobel Ödülleri Ekim ayının başında açıklandı ve meraklı bekleyiş -bu yıl için- sona erdi. Bu seneki Nobel Kimya Ödülü sahiplerine bakacak olursak, kimya camiasında ekseriyetle “çoktan hak edilmişti” düşüncesiyle iç içe geçmiş bir memnuniyet hissi yarattığını söylemek yanlış olmayacaktır. ABD’de Stanford Üniversitesi’nden Carolyn R. Bertozzi ve Scripps Araştırma Enstitüsü’nden K. Barry Sharpless ile Danimarka’da Kopenhag Üniversitesi’nden Morten Meldal arasında eşit olarak paylaştırılan ödül, Türkçe’ye çıtçıt veya klik kimyası olarak çevrilen “click” kimyası ile biyoortogonal kimyanın geliştirilmesi çalışmalarına verildi.
Ayrıntılara girmeden ödülün konusu sorulsa “kavramlarla düşünmenin sonucu olarak geliştirilen belirli organik tepkime sınıflarının kimyanın ve kimyasal biyolojinin çok çeşitli alanlarında çığır açıcı uygulamalar bulması” diyebiliriz sanırım. Gerçekten de hem klik kimyası hem de biyoortogonal kimya önce kavramsal düzeyde ortaya atılmış, sonrasında ise hızla ve çok çeşitli uygulama alanları bulmuşlardır.
Sharpless “klik” kimyası fikrini ortaya atıyor

Barry Sharpless, çalışma arkadaşları H. C. Kolb ve M. G. Finn ile 2001’de yayımladığı ve genel itibariyle şaşkınlık uyandıran ünlü makalesinde “klik” kimyası kavramını öne sürdü.[1]Kolb, H. C.; Finn, M. G.; Sharpless, K. B. (2001) “Click Chemistry: Diverse Chemical Function from a Few Good Reactions” Angew. Chem. Int. Ed., 40, 2004-2021. Bu makaledeki ana argüman, organik kimyada bilinen yüzlerce tepkime çeşidi olmasına rağmen geniş uygulama alanı olan, başarıyla çalışma ihtimali yüksek, güvenilir tepkime sayısının çok az olmasıydı. Dolayısıyla, bu tür tepkime çeşitleri belirlenmeli ve daha da önemlisi bu kıstaslara uyan yeni tepkimeler geliştirilmeliydi.
Fakat önce bu tür tepkimelerin tanımı yapılmalı ve kriterleri ayrıntılı bir şekilde ortaya konmalıydı. Sharpless, önce bu tepkimelere bir kavramsal çerçeve çizdi ve “klik” kimyası terimini ortaya attı. Nasıl bir asma kilidi veya emniyet kemerini taktığınızda, bir kapıyı kapattığınızda veya parçaları uyan iki sert cismi birbirine geçirdiğinizde “klik” sesi duyuluyorsa, iki molekülün birbiriyle kolaylıkla etkileşerek yeni bir ürün oluşturduğu tepkimelere de “klik” tepkimeleri adı verildi. Sharpless’ın önerdiği kriterlere göre, bir tepkimenin çıtçıt (klik) kimyası kategorisine girebilmesi için o tepkime:
-
- Modüler olmalı, yani kolayca modifiye edilebilecek bileşenler içermeli,
- Geniş bir substrat kapsamına sahip olmalı, yani kısıtlı bir sayıda substratla değil de çok çeşitli elektronik özelliklere sahip substratlarla başarılı bir şekilde çalışmalı,
- Tepkimede yan ürünler oluşuyorsa bunlar kolay uzaklaştırılabilen yan ürünler olmalı,
- Tek bir ürün verecek şekilde yüksek verimle çalışmalı,
- Basit tepkime koşulları gerektirmeli,
- Kolay erişilebilir başlangıç maddeleriyle çalışmalı,
- Oluşan ürün kolaylıkla izole edilebilmeli,
- Biyolojik uygulamalarda kullanılacaksa, su ve oksijeni tolere edebilmeli, yani su ve oksijen bulunan ortamlarda da başarıyla çalışabilmelidir.
Keşifler başlıyor
Yukarıda bahsi geçen makalede çıtçıt (klik) kimyası kriterlerine uyan bazı tepkimelerden örnekler verilse de bu alandaki asıl heyecan verici gelişmeler 2002’de yaşandı ve klik kimyası deyince ilk akla gelen tepkimelerden olan “bakır(I)-katalizörlüğünde azit-alkin siklokatılma” tepkimesi keşfedildi. Şekil 1’e bir bakalım:
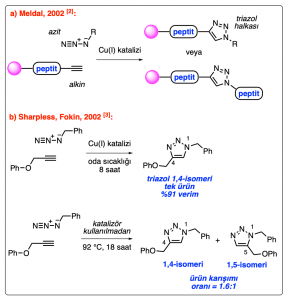

Önce, Morten Meldal ve araştırma grubu, organik azitler (R-N3) ve alkinler (R-C≡CH) arasındaki siklokatılma (halkasal yapı oluşturacak şekilde birbirine bağlanma) tepkimesinin Cu(I) tuzları tarafından katalizlenebildiğini gösterdi (Şekil 1a).[2]Tornøe, C. W.; Christensen, C.; Meldal, M. (2002) “Peptotriazoles on Solid Phase: [1,2,3]-Triazoles by Regiospecific Copper(I)-Catalyzed 1,3-Dipolar Cycloadditions of Terminal Alkynes to Azides” J. Org. Chem. 67, 3057-3064. Beş atomlu bir halkaya sahip triazol ürünlerinin ılımlı koşullar altında kolaylıkla elde edilebildiği bu yöntem birçok peptitin modifikasyonunda kullanıldı.
Çok benzer bir tepkimeyi bu çalışmayla neredeyse eşzamanlı bir şekilde rapor eden başka bir makale ise Barry Sharpless, Valery Fokin ve çalışma arkadaşları tarafından 2002’de yayımlandı.[3]Rostovtsev, V. V.; Green, L. G.; Fokin, V. V.; Sharpless, K. B. (2002) “A Stepwise Huisgen Cycloaddition Process: Copper(I)-Catalyzed Regioselective “Ligation” of Azides and Terminal Alkynes” Angew. Chem. Int. Ed., 41, 2596-2599. Yine Cu(I) katalizi ile organik azitler ve alkinler arasında gerçekleşen bu tepkime oda sıcaklığında yüksek verimlerle yürümekte ve 1,4-izomeri diye adlandırılan triazol ürününü tek ürün olarak vermekteydi (Şekil 1b). Bu yöntem kısa zamanda CuAAC (bakır(I)-katalizörlüğünde azit-alkin siklokatılma) tepkimesi ismiyle ün kazandı.
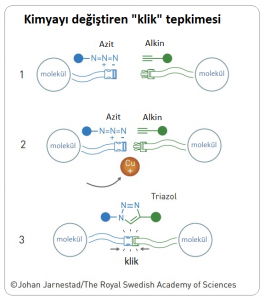
Gerçekten de bu katalitik tepkime, çıtçıt (klik) kimyasının gerekli bütün kriterlerini karşılıyordu ve ne zaman bir araştırmada iki molekül birbirine kolaylıkla ve yüksek verimle bağlanmak istense bu CuAAC tepkimesine başvurulmaya başlandı (Şekil 2).
Çıtçıt terimi tam da bunu anlatıyor. Aynı iki kumaş parçasını birbirine tutturmak için kullanılan çıtçıt gibi: burada çıtçıtın iki parçası moleküller üzerinde bulunan azit ve alkin gruplarına, bu çıtçıt parçalarının birbirine bağlanarak çıtçıtın kapanması ise CuAAC tepkimesine karşılık geliyor. Bu tepkimenin önemini son yirmi yılda ilaç kimyasından kimyasal biyolojiye, malzeme biliminden polimer kimyasına, radyokimyadan supramoleküler kimyaya uzanan çok geniş bir yelpazede oldukça yaygın bir şekilde kullanılmasından da anlayabiliyoruz.[4]Moses, J. E., Moorhouse, A. D. (2007) “The Growing Applications of Click Chemistry” Chem. Soc. Rev., 36, 1249-1262.
Aslında, alkinler ve azitler arasındaki bu tepkime, 1,3-dipolar siklokatılma tepkimeleri adı verilen çok geniş bir tepkime sınıfının bir üyesiydi ve 2020 yılında vefat eden ünlü Alman organik kimyacı Rolf Huisgen tarafından 1960’lı yıllarda incelenmişti.[5]Huisgen, R. (1963) “1,3-Dipolar Cycloadditions. Past and Future” Angew. Chem. Int. Ed., 2, 565-598. Fakat katalitik olmayan bu tepkimeler genellikle yavaştı, yüksek sıcaklık gerektiriyordu ve tek bir ürün vermek yerine bir ürün karışımı oluşturuyordu (Şekil 1b). Bu sebeplerden dolayı, azit-alkin siklokatılma tepkimesinin kimyanın hemen her alanında uygulama şansı bulması, tepkimenin Cu(I) ile katalizlenebildiğinin Meldal ve Sharpless grupları tarafından gösterilmesi sayesinde olmuştur.
Bu noktada aklınıza 1960’lardan beri bilinen azit-alkin siklokatılma tepkimesinin kimyada yaygınlaşmasının niçin bunca yıl geciktiği sorusu gelebilir ki bu çok haklı bir soru olur. Sharpless bunu “azidofobi” diye adlandırdığı bir çeşit kimyevi fobiyle açıklıyor.[6]Kolb, H. C.; Finn, M. G.; Sharpless, K. B. (2001) “Click Chemistry: Diverse Chemical Function from a Few Good Reactions” Angew. Chem. Int. Ed., 40, 2004-2021. Gerçekten de bazı azitlerin kısmi patlayıcı özelliğinden dolayı kimyagerlerde azitlerin kullanımına karşı belli bir çekince mevcuttur. İnorganik bir azit bileşiği olan sodyum azit (NaN3) geçmişte otomobillerin hava yastıklarında kullanılmış olan bir kimyasaldır. Kaza anında bozunarak azot gazı oluşturur ve böyle hava yastığının şişmesini sağlar. Organik bileşiklerde ise özellikle alifatik gruplar içeren organik azitler -molekül ağırlıkları çok düşük olmadığı sürece- görece güvenlidirler. CuAAC tepkimesinin son yirmi yılda çok yaygın bir şekilde ve başarıyla kullanılması, azit içeren bileşiklere karşı olan bu fobiyi büyük ölçüde kırmıştır.
Biyokimyasal süreçleri bozmadan biyomolekülleri incelemenin yolu: Biyoortogonal tepkimeler

2000’li yılların başında çıtçıt (klik) kimyası evreninde tüm bu gelişmeler yaşanırken, biyoortogonal tepkimeler evreninden eşzamanlı başka heyecan verici haberler geliyordu.
Bu alanda en önemli çalışmaları ortaya koyan Carolyn Bertozzi’nin ana araştırma alanı karbohidratların yapılarını ve fonksiyonlarını inceleyen glikobilim (glycoscience) alanıydı. Canlılarda karbohidratların enerji verme ve enerji depolama görevleri ile selülozda olduğu gibi yapısal rollerinin dışında çok önemli bir başka görev alanı daha vardır: Hücre yüzeylerinde bulunan çok çeşitli karbohidratlar (glikanlar), hücre-hücre iletişiminde ve hücrelerin başka molekülleri veya hücreleri tanımasında doğrudan görev alırlar.
1990’ların sonunda bu tür hücre yüzeyinde bulunan glikanları, onları bozmadan incelemek ve görüntülemek için gerekli teknikler mevcut değildi. Bu eksikliğin önemini gören Carolyn Bertozzi de sorunu çözmek üzere bir seri yeni tepkime ve teknik geliştirdi. Biyoortogonal terimi işte bu teknikler için kullanılıyor, biyomoleküllerle etkileşmeyen, biyokimyasal süreçleri bozmayan, yani onlara ortogonal (dikey) olan tepkimeler bunlar.
Bertozzi grubu, 2000’de Science dergisinde yayımladığı bir çalışmada, organik azitler ve fosfinler (R3P şeklinde gösterilebilecek fosfor içeren organik bileşikler) arasındaki Staudinger tepkimesi olarak bilinen tepkimede zekice bir modifikasyon yaparak şimdi Staudinger-Bertozzi bağlama tepkimesi olarak da bilinen tepkimeyi geliştirdi ve bunu hücre yüzeyindeki glikanların seçici bir şekilde modifiye edilebilmesinde kullandı.[7]Saxon, E.; Bertozzi, C. R. (2000) “Cell Surface Engineering by a Modified Staudinger Reaction” Science, 287, 2007-2010. Burada seçicilikten kasıt, hücre yüzeyinde veya içinde bulunan çok sayıdaki başka biyomoleküllerin değil de sadece hedeflenen glikanın tepkimeye girmesi. Bu tepkime başarıyla çalışmasına rağmen yavaş ilerleyen bir tepkimeydi ve dolayısıyla, hücredeki belirli süreçlerin görüntülenmesinde hızı açısından yetersiz kalıyordu.
Meldal ve Sharpless grupları tarafından 2002’de geliştirilen CuAAC tepkimesi hem hızı hem de seçiciliği bakımından Bertozzi’nin yapmak istediği çalışmalar için ideal bir tepkime adayıydı. Buradaki tek sorun ise bu tepkimenin ılımlı koşullarda gerçekleşmesi için gerekli olan bakır iyonlarının hücreler için toksik özellik göstermesiydi.
Bu noktada, Bertozzi bu alanda çığır açan bir çözüm ortaya koydu: Tepkimede alkin bileşeni olarak sekiz karbonlu halkasal bir alkin olan siklooktin bileşiğini kullandı. Alkinler, doğaları gereği doğrusal geometriye sahip olmak isterler ve dolayısıyla, bir halka içindeyken mutlu değildirler. Bu da halkasal alkinlerin yüksek enerjili olmalarına yol açar ve buna “halka gerginliği” denir. Siklooktin, izole edilebilir, en küçük sayıda karbon içeren sikloalkindir. Bertozzi ve grubu, halka gerginliğini üzerinden atmak için tepkimeye girmeye hevesli olan bu bileşiğin, Cu(I) katalizörüne gerek kalmadan organik bir azitle oda sıcaklığında kolaylıkla tepkimeye girebildiğini gösterdi.[8]Agard, N. J.; Prescher, J. A.; Bertozzi, C. R. (2004) “A Strain-Promoted [3+2] Azide-Alkyne Cycloaddition for Covalent Modification of Biomolecules in Living Systems” J. Am. Chem. Soc., 126, 15046-15047. Hem bu tepkimenin hem de yukarıda bahsedilen Staudinger-Bertozzi tepkimesinin ortak özelliği biyoortogonal olmasıydı. Bu tepkimelerde kullanılan fonksiyonel gruplar olan azit, alkin ve fosfin grupları canlılarda ya hiç olmayan ya da çok ender rastlanan fonksiyonel gruplardır ve dolayısıyla bunları içeren bir tepkime canlılardaki diğer biyomoleküllerle etkileşmeyecek yani onlara ortogonal olacaktır.
Biyoortogonal tepkimelerin kavramsal olarak Bertozzi tarafından ortaya atılması, araştırmacıların düşünme tarzını derinden etkilemiş ve ilerleyen yıllarda yeni biyoortogonal tepkimelerin keşfinin önünü açmıştır.
Şekil 3’te biyoortogonal bir çıtçıt tepkimesinin örneği şematik olarak gösteriliyor. Bu örnekte, çıtçıtın bir ucu olan azit grubu hücre yüzeyindeki bir glikan ünitesine, çıtçıtın diğer ucu olan siklooktin ise floresan bir moleküle bağlı. Çıtçıt tepkimesiyle floresan molekülün şeker içeren proteine (glikoprotein) bağlanması sağlanıyor ve proteinin görüntülenmesi mümkün oluyor.
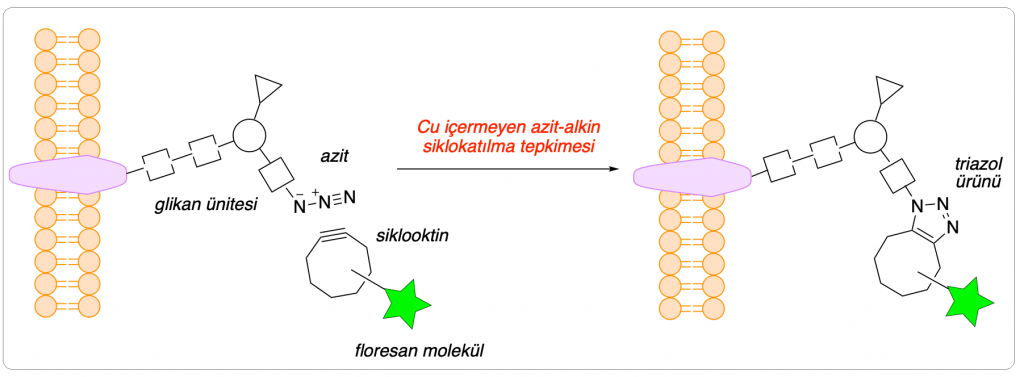
Özetle, Bertozzi’nin geliştirdiği bu teknik, hücrelerde veya canlı organizmalarda ne zaman iki (biyo)molekül birbirine seçici bir şekilde bağlanmak istense tercih edilen yöntem oldu ve kimyasal biyolojide çok çeşitli uygulamalarda kullanıldı.
Sharpless ikiledi
Son olarak bu ödülün, Barry Sharpless’ın kimya alanında aldığı ikinci Nobel Ödülü olduğunu vurgulamakta fayda var. İlkini, 2001 yılında asimetrik (enantiyo-seçici) yükseltgenme tepkimeleri üzerine yaptığı çalışmalarla almış ve ödülü diğer bilim insanları Ryoji Noyori ve William Knowles ile paylaşmıştı.
Geçmişte Kimya Nobel Ödülü’nü almaya bu şekilde iki kez hak kazanan bir isim daha bulunuyor: Frederick Sanger. Proteinlerin amino asit dizilimini belirlemeye yönelik geliştirdiği yöntemle 1958 Nobel Kimya Ödülü’nü kazanan Sanger, DNA sekanslama çalışmaları ile de aynı dalda 1980 Nobel Ödülü’ne hak kazandı.
Bu noktada aklınıza büyük ihtimalle meşhur Marie Skłodowska-Curie gelmiştir. Nobel Ödülü’nü benzer şekilde iki kez kazanan Curie bu ödüllerden ilkini 1903’te fizik alanında alırken, ikincisini 1911’de kimya alanında almıştı. Yine kimya tarihinin en önemli isimlerinden Linus Pauling, 1954’te Nobel Kimya Ödülü’yle ödüllendirilirken, Doğu ve Batı arasındaki nükleer silahlanma yarışına karşı yaptığı barış çalışmalarıyla 1962’de Nobel Barış Ödülü’nü almıştır.
Yunus Türkmen
Bilkent Üniversitesi Kimya Bölümü
Notlar/Kaynaklar
| ↑1, ↑6 | Kolb, H. C.; Finn, M. G.; Sharpless, K. B. (2001) “Click Chemistry: Diverse Chemical Function from a Few Good Reactions” Angew. Chem. Int. Ed., 40, 2004-2021. |
|---|---|
| ↑2 | Tornøe, C. W.; Christensen, C.; Meldal, M. (2002) “Peptotriazoles on Solid Phase: [1,2,3]-Triazoles by Regiospecific Copper(I)-Catalyzed 1,3-Dipolar Cycloadditions of Terminal Alkynes to Azides” J. Org. Chem. 67, 3057-3064. |
| ↑3 | Rostovtsev, V. V.; Green, L. G.; Fokin, V. V.; Sharpless, K. B. (2002) “A Stepwise Huisgen Cycloaddition Process: Copper(I)-Catalyzed Regioselective “Ligation” of Azides and Terminal Alkynes” Angew. Chem. Int. Ed., 41, 2596-2599. |
| ↑4 | Moses, J. E., Moorhouse, A. D. (2007) “The Growing Applications of Click Chemistry” Chem. Soc. Rev., 36, 1249-1262. |
| ↑5 | Huisgen, R. (1963) “1,3-Dipolar Cycloadditions. Past and Future” Angew. Chem. Int. Ed., 2, 565-598. |
| ↑7 | Saxon, E.; Bertozzi, C. R. (2000) “Cell Surface Engineering by a Modified Staudinger Reaction” Science, 287, 2007-2010. |
| ↑8 | Agard, N. J.; Prescher, J. A.; Bertozzi, C. R. (2004) “A Strain-Promoted [3+2] Azide-Alkyne Cycloaddition for Covalent Modification of Biomolecules in Living Systems” J. Am. Chem. Soc., 126, 15046-15047. |